Antybiotyk (z gr. anti, znaczy przeciw i bios, czyli życie) to produkt metabolizmu mikroorganizmów, wpływający na struktury komórkowe i procesy metaboliczne innych mikroorganizmów, czyli bakterii, dermatofitów, pleśni i drożdżaków, za wyjątkiem, co należy zaakcentować, wirusów, które nie są zaliczane do organizmów, jako m.in. niezdolne do samodzielnego namnażania.
Podobno od czasu wynalezienia pierwszego antybiotyku, czyli legendarnej już dziś penicyliny, antybiotyki uratowały ok. stu milionów istnień ludzkich. Zanim zaczęto je stosować ok. 40 % ludności Ziemi umierało z powodu różnego rodzaju infekcji, w tym regularnie nawiedzających ludzkość chorób bakteryjnych, takich jak cholera, tyfus, dżuma, czy gruźlica.
Początki odkryć mikrobiologicznych, w tym bogatego świata bakterii, to czasy stosunkowo nieodległe, zaledwie koniec XVI wieku, a były związane z wynalezieniem mikroskopu. Określenie mikroskop pochodzi od starogreckich słów: mikros, czyli mały oraz skopeo – patrzę, obserwuję, ponieważ rzeczywiście jest to urządzenia umożliwiające wejrzenie w świat niedostępnych gołym okiem mikroorganizmów. Przełomem było skonstruowanie w roku 1590 pierwszego mikroskopu przez holenderskich optyków Hansa oraz Zachariasa Janssenów (ojca i syna), który składał się z dwóch soczewek. Janssenom przypisuje się także wynalezienie teleskopu. Pierwsze „prawdziwe” obserwacje mikroskopowe (w latach 1665-1667) przeprowadził angielski przyrodnik Robert Hooke. Natomiast w 1676 roku holenderski urzędnik miejski, przedsiębiorca i przyrodnik amator Antoni van Leeuwenhoek skonstruował mikroskop powiększający prawie trzystukrotnie, co znacznie zwiększyło możliwości obserwacji. Pomysłowy Holender m.in. obalił teorię samorództwa po dokonaniu odkrycia, że muchy składają jaja; zaobserwował również "żyjątka" bytujące na zębach.

fot. 1
Zacharias Janssen

fot. 2
Robert Hooke

fot. 3
Antoni van Leeuwenhoek
Wiekopomnego dla ludzkości odkrycia dokonał w 1928 roku Alexander Fleming, szkocki bakteriolog i lekarz, a także późniejszy laureat Nagrody Nobla w dziedzinie medycyny. Jak to się zdarza w przypadku największych odkryć naukowych, dokonał go przez przypadek, w trakcie sprzątania laboratorium, kiedy to zaobserwował zatrzymanie wzrostu kultur bakterii z rodzaju Staphylococcus poprzez przypadkowe zanieczyszczenie podłoża naczynia laboratoryjnego pleśnią Penicillium notatum.
Dokonana obserwacja była na tyle intrygująca, że poświęcił jej kolejnych kilka lat, w efekcie odkrywając działającą silnie bakteriobójczo penicylinę G, która jednocześnie nie stanowiła dużego obciążenia dla organizmu człowieka, więc okazała się znakomitym medykamentem. Niestety z powodu braku środków finansowych, badania zostały wstrzymane, dlatego przeniósł się do USA, aby tam kontynuować pracę badawczą.
Z biegiem lat odkryto następne pokolenia antybiotyków naturalnych, półsyntetycznych i syntetycznych. Odkryto też, że oprócz pleśni zdolnością wytwarzania antybiotyków wyróżniają się promieniowce oraz niektóre bakterie. W przeciągu całego XX wieku odkryto jedynie siedem grup antybiotyków, natomiast od ponad trzydziestu lat nie pojawił się żaden nowy rodzaj. I pewnie ten stan nie ulegnie szybko zmianie, ponieważ odkrycie nowego antybiotyku zajmuje ok. 8-10 lat.

fot. 4
Alexander Fleming
fot. 5
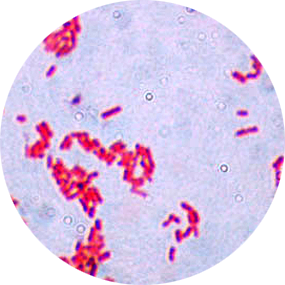
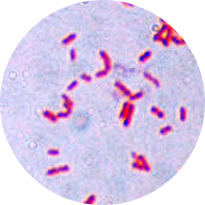
Pałeczka okrężnicy
Aktualnie jednym z największych globalnych problemów medycznych jest zwiększanie się lekooporności wielu szczepów bakteryjnych, w wyniku ich nadużywania oraz nieprawidłowego stosowania przez pacjentów. Zdarza się, że lekarz internista lub pediatra, przepisuje antybiotyki w przypadku podejrzenia choroby wirusowej, ponieważ pacjent wręcz na nim to wymusza, sam sobie lub swojemu dziecku nieświadomie szkodząc. Jednakże praktyka przepisywania antybiotyków w przypadku chorób wirusowych podyktowana jest również możliwością powstania nadkażenia bakteryjnego, szczególnie w przypadku infekcji przewlekłych, czego lekarz nie powinien zbagatelizować. Dlatego decyzja odnośnie ewentualnego przepisania antybiotyku zależy wyłącznie od lekarza, biorącego pod uwagę różnego rodzaju czynniki.
Współcześnie największe wyzwanie w zakresie leczenia chorób bakteryjnych stanowią szczepy wielooporne, wśród których występują odmiany niewrażliwe na żaden z dostępnych leków. Oporność bakterii na lek stwierdza się w przypadku, kiedy średnie stężenia antybiotyków niszczące populację drobnoustrojów in vitro (łac. dosłownie znaczy w szkle, a oznacza procesy biologiczne przeprowadzane w warunkach laboratoryjnych, poza organizmem) jest większe od stężeń uzyskanych in vivo (łac. znaczy na żywym, odnosi się do zjawiska w żywym organizmie). Oznacza to po prostu, że podczas eksperymentów medycznych, w celu likwidacji danej populacji bakterii, konieczne jest stosowanie większej ilości antybiotyku.
Podstawowym typem oporności wykazywanym przez bakterie jest oporność naturalna, czyli wrodzona oporność na niektóre grupy antybiotyków. Jej przeciwieństwem jest oporność nabyta, powstająca u bakterii, które pierwotnie były wrażliwe na dany lek, a która pojawiła się w wyniku kontaktu z danym antybiotykiem podczas niewłaściwego lub zbyt krótkiego stosowania medykamentu. Oprócz niewłaściwego stosowania preparatów leczniczych, źródłem lekooporności jest również woda skażona ściekami kanalizacyjnymi oraz odchodami zwierząt, w których hodowli stosuje się na dużą skalę antybiotyki.
E. coli, czyli pałeczka okrężnicy, wchodzi w skład flory bakteryjnej jelita grubego, uczestnicząc w rozkładzie pokarmu oraz przyczyniając się do produkcji witamin z grupy B i K, jednakże w określonych okolicznościach może wykazywać właściwości chorobotwórcze, wywołując schorzenia układu pokarmowego oraz moczowego.
Kilka lat temu naukowcy tureccy i amerykańscy stworzyli sztuczną populację bakterii E. coli, u której próbowali uzyskać odporność na podstawowe antybiotyki, w efekcie otrzymując oporność krzyżową, czyli niewrażliwość na wszystkie antybiotyki z danej grupy, mimo teoretycznego nabycia odporności tylko na jeden z nich. Wynik eksperymentu był zaskakujący, ponieważ lekooporność krzyżową bakterii obserwowano dotychczas na antybiotyki z grupy makrolidów, np. erytromycynę. Uzmysłowiło to badaczom, że bakterie mogą szybko ewoluować, zyskując nowe umiejętności, stanowiące prawdziwe zagrożenie dla ludzkiej populacji.
Bakteriofagi, czyli wirusy atakujące bakterie, to nasi nieożywieni sprzymierzeńcy w mikroświecie, o których istnieniu dowiedzieliśmy się w 1896 roku, kiedy to angielski bakteriolog Ernest Hanbury Hankin opublikował artykuł, w którym informował o odkryciu w badanych przez siebie wodach Gangesu w Indiach, niewidzialnych gołym okiem czynników antybakteryjnych. Praca nie została jednak zauważona i dopiero dwadzieścia lat później wykryto owe czynniki, czyli bakteriofagi (to znaczy „zjadacze bakterii”).
fot. 6
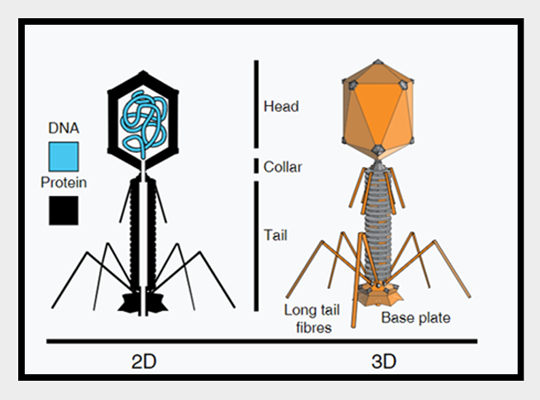
Bakteriofag

fot. 7
Miasto Varanasi nad Gangesem w Indiach
Nazwa zaproponowana przez pracującego w Paryżu Kanadyjczyka Félixa d’Herell jest efektowna, ale przekłamuje rzeczywistość, ponieważ wirusy, nie będąc żywymi organizmami, w rzeczywistości niczego nie pożerają. Fagi wkłuwają się do wnętrza bakterii i wstrzykują tam swój materiał genetyczny, doprowadzając do replikacji własnego genomu. Zainfekowana komórka replikuje wirusy aż ulega rozerwaniu uwalniając nowe wirusy, co jest procesem bardzo szybkim, zajmującym ok. trzydziestu minut.

fot. 8
Ernest Hanbury Hankin

fot. 9
Félix d’Herell
Pierwszą kurację bakteriofagami, skierowaną przeciw laseczkom czerwonki, czyli patogenom powodującym groźną dezynterię, zastosowano 1915 roku. Następne lata tylko potwierdziły skuteczność metody, jednak odkrycie antybiotyków oraz ich masowa produkcja spowodowały zmniejszenie zainteresowania nią wśród lekarzy. W obliczu rozwoju lekooporności wielu szczepów bakterii, niektórzy badacze rozważają powrót do stosowania fagów, co wydaje się bardzo obiecujące, ponieważ na fagi nie można się uodpornić, gdyż mutują bardzo szybko. Ponadto leczenie fagami jest bezpieczne, ponieważ nie powoduje skutków ubocznych. Wirusy działają wybiórczo – każdy gatunek bakterii ma swojego faga - dlatego określony bakteriofag atakuje tylko jeden gatunek bakterii. Obecnie metoda leczenia fagami jest stosowana tylko w dwóch krajach na świecie – w Polsce oraz Gruzji - co stanowi dla naszego kraju duże wyróżnienie. Jednakże nawet w tych dwóch krajach stosowanie bakteriofagów ograniczone jest tylko do wybranych ośrodków naukowych, gdyż nie jest to metoda powszechna.
Na tytułowe pytanie można odpowiedzieć, że antybiotyki jako skuteczne medycznie produkty metabolizmu mikroorganizmów chronią nasze życie przed zagrażającymi nam patogenami. Jednakże zaistnienie zjawiska lekooporności wielu szczepów bakteryjnych spowodowało ograniczenie tej metody oraz potrzebę poszukiwania innych lub powrotu do terapii częściowo zapomnianych, takich jak wspomniana terapia bakteriofagowa.
Anita Karykowska
Public Relations, SPZZLO Warszawa-Żoliborz
Copyrights 2024 | Samodzielny Publiczny Zespół Zakładów Lecznictwa Otwartego Warszawa Żoliborz-Bielany | Wszelkie Prawa Zastrzeżone. Kopiowanie, przetwarzanie i rozpowszechnianie tych materiałow w całosci lub w części bez zgody właściciela jest zabronione i stanowi naruszenie praw autorskich.